O nás
Projekt se zaměřuje na vývoj nových protirakovinných látek, které selektivně působí proti maligně transformovaným buňkám.
Výzkumné cíle:
- navrhnout, připravit a otestovat účinné protinádorové látky, zvláště s ohledem na selektivní zabíjení maligních buněk;
- analyzovat a porozumět molekulární biologii rakovinných kmenových buněk a jejich rezistenci vůči apoptóze;
- navrhnout a ověřit efektivní terapeutickou strategii pro použití v klinické medicíně vedoucí k minimalizaci nádorových relapsů.
Laboratoř Molekulární terapie nádorů se zaměřuje na navrhování a vývoj nových protirakovinných látek, zejména analogů vitaminu E, které jsou účinné a selektivní pro maligní buňky. Je zde zejména vědecký zájem o molekulární mechanismy apoptózy vyvolané takovými látkami, které zahrnují dráhy mitochondriální destabilizace. Byly definovány a charakterizovány takzvané mitokany, nízkomolekulární látky vykazující protirakovinnou aktivitu prostřednictvím mitochondrií. Tyto látky jsou pozoruhodné zejména z translačního pohledu, jelikož nyní už je zřejmé, že nádory jsou vysoce heterogenní z hlediska mutací, dokonce v různých oblastech téhož nádoru. A mitochondrie mohou představovat stabilní cíl využitelný pro terapii rakoviny.
V laboratoři se zkoumají zejména mitokany ze skupiny analogů vitaminu E, reprezentované redoxně neaktivním α-tokoferylsukcinátem (α-TOS). Tato látka vykazuje vysokou apoptogenní aktivitu v mnoha liniích rakovinných buněk, zatímco je netoxická pro normální buňky. Tato in vitro proapoptotická aktivita má obdobu v protirakovinné aktivitě in vivo u myších modelů nádorů, což bylo prokázáno pro nádory konečníku, prsu a mezoteliomy. Tímto nálezem získává α-TOS značný translační význam a stává se výchozí látkou pro vývoj účinnějších agens.
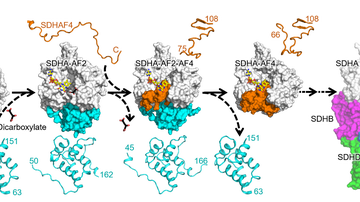
Ve snaze charakterizovat dráhy regulující přenos apoptotických signálů v rakovinných buňkách spouštěný α-TOSem, objevili Neužil a spol. nový cíl protirakovinných léčiv, mitochondriální komplex II (CII). Zjistili, že α-TOS a podobné látky interagují s proximálním i distálním vazebným místem CII pro ubichinon (UbQ), a tím v CII UbQ nahrazují. CII, působením své sukcinátdehydrogenázové (SDH) aktivity, převádí sukcinát na fumarát, jakožto komponenta cyklu trikarbonových kyselin (TCA). Elektrony uvolněné touto reakcí jsou normálně převzaty UbQ a předány na CIII elektron-transportního řetězce (ETC), součást oxidativní fosforylace. V případě, že UbQ je nahrazen α-TOSem nebo podobnými látkami, elektrony reagují s molekulárním kyslíkem a způsobí vznik superoxidu, čímž zapínají apoptotickou signální kaskádu. Jelikož geny kódující subjednotky CII mutují zcela výjimečně, komplex představuje velmi slibný cíl pro protirakovinná léčiva.
V úsilí zvýšit apoptogenní aktivitu α-TOSu byla látka modifikována připojením kationtové trifenylfosfoniové (TPP) skupiny, která způsobí akumulaci činidla (mitochondriálně zacílený sukcinát vitaminu E, MitoVES) mezi mitochondriální vnitřní membránou a mitochondriální matrix. Tím se zvýší apoptogenní aktivita rodičovské látky o 1-2 řády. Je důležité, že tento vzestup toxicity vůči rakovinným buňkám neovlivní selektivitu látky pro maligní buňky. Přístup laboratoře k terapii rakoviny pomocí přivěšení lipofilních kationtů (jako je TPP) k protirakovinným agens představuje nový vzor účinné léčby rakoviny. Ve skupině dále pokračují v této linii výzkumu, aby syntetizovali nové, účinnější protirakovinné látky zacílené na mitochondrie. Zejména plánují započít translační výzkum, na jehož základě by předali jejich nová léčiva do klinické praxe. V případě úspěchu by to mohlo úplně změnit dosavadní i budoucí terapeutické způsoby a potenciálně vést k opravdu účinné léčbě rakoviny.